GLP-1 et Glucagon : les hormones digestives clés pour une perte de poids durable
Rédaction : Anne-Christine DUSS, Nutritionniste
1. La nouvelle frontière hormonale de la perte de poids
Pendant des décennies, la perte de poids a été envisagée sous un angle purement calorique : il suffisait, pensait-on, de “manger moins et bouger plus”. Pourtant, la science du métabolisme a montré que le corps humain ne fonctionne pas comme une simple balance énergétique. Derrière chaque kilo perdu ou repris se cache une orchestration hormonale complexe, où la faim, la satiété, le stockage et la combustion des graisses sont finement régulés par le système endocrinien.
C’est dans ce contexte que c, ont émergé comme des acteurs centraux du contrôle du poids corporel. Ces molécules, naturellement produites par notre corps, participent à un dialogue constant entre l’intestin, le pancréas, le cerveau et le foie. Ensemble, elles dictent quand nous avons faim, quand nous devons stocker l’énergie, et quand nous pouvons la libérer pour bouger ou maintenir notre température corporelle.
Cette compréhension ouvre une voie nouvelle : celle d’une perte de poids durable et physiologique, non pas obtenue par la privation, mais par la stimulation naturelle des hormones régulatrices du métabolisme.
Alors que le marché des médicaments agonistes du GLP-1 (comme le semaglutide ou le liraglutide) explose à l’échelle mondiale, la véritable révolution se joue peut-être ailleurs : dans la reconnexion du corps à ses signaux hormonaux naturels, par l’alimentation, l’activité physique et la régulation du stress.
Pour comprendre cette révolution, il faut d’abord savoir comment fonctionnent le GLP-1 et le glucagon, et pourquoi leur équilibre est essentiel pour maintenir un poids stable et une énergie constante.
2. Comprendre le GLP-1 et le glucagon : un duo clé du métabolisme
Le GLP-1 et le glucagon peuvent être vus comme deux faces d’une même médaille :
- l’un favorise la satiété et le stockage,
- l’autre stimule la libération d’énergie et la combustion des graisses.
Ensemble, ils permettent au corps de naviguer entre état de jeûne et état postprandial (après repas), assurant la stabilité du poids et de la glycémie.
Le GLP-1 : messager intestinal de la satiété
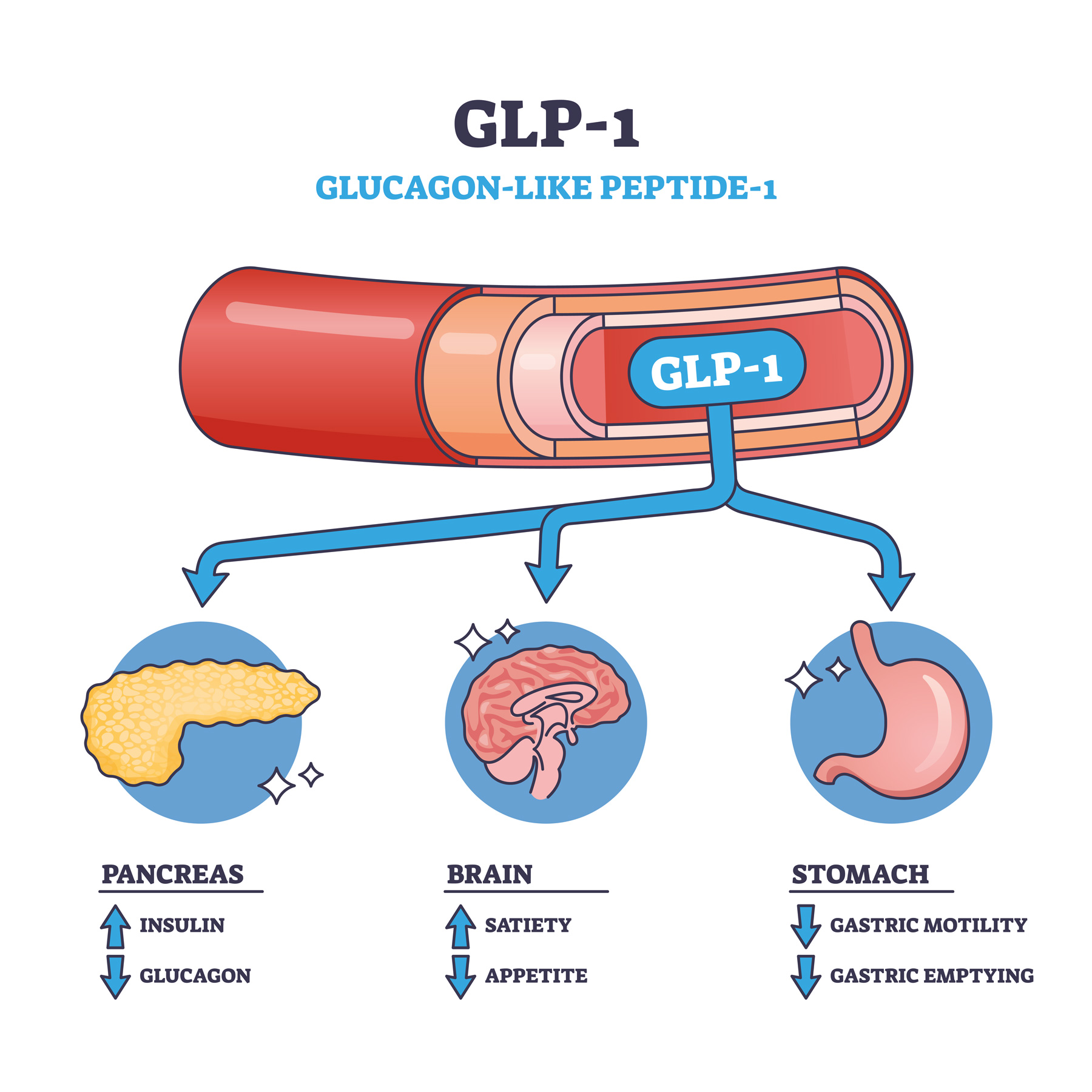
Le GLP-1 est produit par les cellules L de l’intestin grêle et du côlon, principalement en réponse à la présence de nutriments, surtout de glucides et de lipides. Une fois libéré dans le sang, il agit sur plusieurs organes :
- Le pancréas, où il stimule la sécrétion d’insuline (pour faire entrer le glucose dans les cellules) et inhibe celle du glucagon (pour éviter une libération excessive de sucre par le foie).
- Le cerveau, où il se fixe sur les récepteurs hypothalamiques et active les zones de satiété, réduisant ainsi la faim et les pulsions alimentaires.
- L’estomac, où il ralentit la vidange gastrique, prolongeant la sensation de plénitude après le repas.
- Le foie, indirectement, en réduisant la production de glucose hépatique.
Ce rôle de “chef d’orchestre” de la satiété fait du GLP-1 une hormone clé de la régulation pondérale naturelle. Plus son activité est efficace, plus le corps parvient à stabiliser son poids sans effort de volonté particulier.
Inversement, un déficit de sécrétion ou de sensibilité au GLP-1 est souvent observé chez les personnes souffrant d’obésité, de résistance à l’insuline ou de troubles du comportement alimentaire.
Le glucagon : moteur du déstockage énergétique
Le glucagon, produit par les cellules α du pancréas, agit de manière complémentaire au GLP-1. Alors que le GLP-1 est libéré après les repas, le glucagon s’active plutôt pendant le jeûne, le sport ou les périodes de stress énergétique.
Son rôle est de libérer les réserves :
- il stimule la glycogénolyse (libération du glucose stocké dans le foie),
- active la lipolyse (dégradation des graisses stockées dans les adipocytes),
- et favorise la néoglucogenèse (production de glucose à partir des acides aminés ou du glycérol).
Le glucagon agit comme un signal d’alerte métabolique, garantissant que le cerveau et les muscles disposent d’énergie entre les repas. Mais il ne s’agit pas d’une hormone “opposée” au GLP-1 : les deux sont étroitement interconnectées. En réalité, le GLP-1 régule le glucagon en fonction du contexte :
- après un repas, il freine sa sécrétion pour éviter un excès de sucre sanguin,
- mais à long terme, il améliore la sensibilité du foie à son action, favorisant ainsi une meilleure combustion des graisses.
Un équilibre à préserver
L’équilibre entre GLP-1 et glucagon est ce qui permet au corps de basculer naturellement entre stockage et déstockage.
Quand cet équilibre est rompu — par une alimentation trop sucrée, un stress chronique ou un manque de sommeil —, le corps devient “sourd” à ses signaux hormonaux :
- la satiété diminue,
- la faim augmente,
- la combustion énergétique ralentit.
C’est ce qu’on observe dans le syndrome métabolique ou l’obésité hormonale : un état où les circuits de satiété et de dépense énergétique sont désynchronisés.
Heureusement, il est possible de réentraîner le corps à libérer ces hormones et à y répondre correctement, par des leviers naturels. C’est ce que nous verrons dans les prochaines sections.
3. Le GLP-1 : chef d’orchestre de la satiété
Le GLP-1 ne se limite pas à une simple régulation glycémique : c’est une hormone multifonction, essentielle pour contrôler la faim, la satiété et la motivation alimentaire. Son rôle peut être résumé en trois axes principaux :
Ralentir la digestion pour prolonger la satiété
L’un des effets les plus tangibles du GLP-1 est son action sur l’estomac. Après un repas, l’hormone ralentit la vidange gastrique, ce qui signifie que les aliments restent plus longtemps dans l’estomac et que la sensation de “plein” persiste.
Cette régulation est cruciale : elle permet de limiter les grignotages et d’espacer les repas naturellement. Des études ont montré que chez des sujets ayant une sécrétion adéquate de GLP-1, la sensation de satiété dure significativement plus longtemps, réduisant spontanément l’apport calorique quotidien (Holst, 2007).
Action sur le cerveau : diminuer la faim et moduler la récompense
Le GLP-1 agit également comme messager vers le cerveau, en particulier l’hypothalamus, centre nerveux qui contrôle la faim et la satiété.
- Il active les neurones anorexigènes qui signalent que le corps a reçu suffisamment d’énergie.
- Il inhibe les neurones orexigènes, responsables de la faim excessive.
- Il module même le système dopaminergique de la récompense alimentaire, diminuant le plaisir associé aux aliments très gras ou sucrés.
En pratique, un taux suffisant de GLP-1 permet de manger moins mais mieux, en réduisant les pulsions alimentaires sans provoquer de frustration.
Interactions avec le microbiote et l’alimentation
Le GLP-1 n’agit pas seul : son efficacité dépend en partie de l’état du microbiote intestinal. Les bactéries digestives fermentent les fibres alimentaires pour produire des acides gras à chaîne courte (AGCC), comme le butyrate ou le propionate. Ces molécules stimulent directement les cellules L, augmentant la libération de GLP-1.
Ainsi, une alimentation riche en fibres solubles, en protéines maigres et en aliments fermentés favorise naturellement la sécrétion de GLP-1 et renforce la régulation de la satiété.
4. Le glucagon : moteur de la combustion énergétique
Si le GLP-1 nous aide à manger moins et mieux, le glucagon nous aide à brûler l’énergie stockée, en particulier les graisses.
Libération d’énergie pendant le jeûne et l’exercice
Le glucagon est principalement sécrété par le pancréas lorsque la glycémie baisse, comme pendant :
- le jeûne nocturne,
- les repas espacés,
- l’exercice physique intense.
Son rôle est de mobiliser les réserves énergétiques pour assurer le fonctionnement optimal des organes vitaux et des muscles. Concrètement, il :
- stimule la glycogénolyse (libération du glucose hépatique),
- active la lipolyse (dégradation des graisses stockées),
- favorise la production de corps cétoniques, utilisés comme carburant alternatif par le cerveau et les muscles.
Complémentarité avec le GLP-1
Le glucagon et le GLP-1 ne sont pas en opposition mais coopèrent pour réguler le métabolisme. Par exemple
- Après un repas, le GLP-1 inhibe partiellement le glucagon pour éviter une hyperglycémie.
- Entre les repas, le glucagon prend le relais pour maintenir la glycémie et mobiliser les graisses, tandis que le GLP-1 prépare le corps à une satiété efficace au prochain repas.
Cet équilibre dynamique permet de passer d’un état de stockage postprandial à un état de déstockage énergétique sans provoquer de déséquilibre hormonal ni de fringales excessives.
Le glucagon et la flexibilité métabolique
La capacité à libérer du glucagon efficacement est un indicateur de flexibilité métabolique : le corps peut passer rapidement d’un mode “stockage” à un mode “combustion” selon les besoins énergétiques.
Une flexibilité métabolique optimale permet de limiter la prise de poids même en période de surplus calorique modéré. À l’inverse, une sécrétion glucagonique faible ou inefficace est associée à une accumulation de graisses, une résistance à l’insuline et une plus grande difficulté à perdre du poids.
Des interventions naturelles, comme le jeûne intermittent, l’entraînement fractionné et une alimentation riche en protéines, peuvent stimuler la libération de glucagon et améliorer cette flexibilité, favorisant ainsi une perte de poids durable.
Pourquoi stimuler ces hormones naturellement ?
Stimuler le GLP-1 et le glucagon de manière naturelle présente plusieurs avantages par rapport aux médicaments :
- Durabilité : le corps apprend à réguler sa satiété et sa combustion énergétique.
- Équilibre physiologique : pas de risque de dépendance hormonale artificielle.
- Amélioration globale de la santé : microbiote, glycémie, lipides et énergie physique sont optimisés simultanément.
En résumé, manger moins mais mieux et brûler les réserves efficacement devient possible en reconnectant notre corps à ses signaux hormonaux naturels.
5. Stimuler naturellement le GLP-1 et le glucagon
Pour une perte de poids durable, il est possible de réactiver ces hormones naturellement grâce à l’alimentation, l’activité physique et des habitudes de vie ciblées. L’idée n’est pas de “forcer” le corps, mais de reconnecter les circuits hormonaux à leur fonctionnement physiologique.
Alimentation
Les nutriments clés qui stimulent le GLP-1 et le glucagon sont :
- Protéines : sources maigres comme le poisson, le poulet, les œufs ou le lactosérum (whey). Les protéines stimulent la sécrétion de GLP-1 et favorisent la libération de glucagon pendant la digestion.
- Fibres solubles : avoine, légumineuses, psyllium, graines de chia. Ces fibres fermentent dans le côlon pour produire des acides gras à chaîne courte (AGCC), comme le butyrate et le propionate, qui stimulent directement les cellules L sécrétrices de GLP-1.
- Aliments fermentés : kéfir, yaourt, choucroute, miso. Ils nourrissent le microbiote et renforcent la production naturelle de GLP-1.
- Polyphénols : thé vert, cacao, fruits rouges, curcuma. Ces molécules améliorent la sensibilité à l’incrétine et la régulation de la glycémie.
Conseil pratique : privilégier des repas composés de protéines, de fibres et de lipides de qualité, à index glycémique bas. Cela stimule le GLP-1 et limite la sécrétion excessive d’insuline, tout en favorisant la combustion des graisses via le glucagon.
Activité physique
L’exercice est un puissant stimulateur hormonal :
- HIIT et musculation : favorisent la libération de glucagon, mobilisant les graisses et améliorant la flexibilité métabolique.
- Exercice modéré : marche rapide, vélo, natation, favorise la sensibilité à l’insuline et à l’action du GLP-1 postprandial.
L’activité physique régulière permet donc de renforcer les deux hormones, optimisant à la fois la satiété et la combustion énergétique.
Jeûne et timing alimentaire
Le jeûne intermittent ou des fenêtres alimentaires restreintes (8-10h) :
augmentent la sécrétion de glucagon entre les repas, mobilisant les réserves énergétiques.
préparent le corps à une réponse plus efficace au GLP-1 au moment du repas suivant, réduisant l’appétit et les envies de sucre.
Sommeil et gestion du stress
Le manque de sommeil et le stress chronique élèvent le cortisol, qui :
- diminue la sensibilité aux hormones de satiété (GLP-1),
- favorise le stockage des graisses abdominales,
- réduit la sécrétion de glucagon en réponse au jeûne.
Pratiques efficaces : 7–8 heures de sommeil, cohérence cardiaque, méditation ou yoga, pour restaurer l’équilibre hormonal naturel.
Suppléments et molécules naturelles
Certaines substances peuvent soutenir la production hormonale :
- Berbérine : améliore la sensibilité à l’insuline et stimule indirectement le GLP-1.
- Curcumine et quercétine : protègent les cellules L et augmentent la sécrétion de GLP-1.
- Caféine modérée : stimule légèrement la libération de GLP-1 et le métabolisme basal.
- Acide alpha-lipoïque et chrome : renforcent la sensibilité hormonale et la régulation glycémique.
Ces approches ne remplacent pas un mode de vie sain, mais peuvent amplifier l’effet des leviers naturels.
6. Quand la médecine imite la nature : les agonistes du GLP-1
Pour les personnes en obésité sévère ou présentant une résistance hormonale importante, les médecins ont développé des médicaments qui miment l’action du GLP-1, appelés agonistes du GLP-1. Les plus connus sont :
- Liraglutide (Saxenda® / Victoza®)
- Semaglutide (Ozempic® / Wegovy®)
- Tirzepatide (Mounjaro®), un agoniste combiné GLP-1/GIP.
Ces médicaments amplifient artificiellement la sensation de satiété, ralentissent la vidange gastrique et améliorent la régulation glycémique.
Efficacité réelle
Les études cliniques montrent :
- Perte de 5 à 10 % du poids corporel avec le liraglutide.
- Perte de 15 % avec le semaglutide.
- Perte jusqu’à 20 % avec le tirzepatide.
Ces chiffres dépassent largement les résultats des régimes classiques ou des modifications de mode de vie seules, expliquant leur succès mondial.
Limites et effets secondaires
Malgré leur efficacité, ces médicaments présentent des contraintes :
- Nausées, vomissements, diarrhées (effets fréquents au début du traitement).
- Fatigue et perte d’appétit excessive, pouvant entraîner un déficit calorique ou protéique.
- Risque de reprise de poids après arrêt du traitement (souvent 50–70 % du poids perdu).
- Perte musculaire si l’apport protéique et l’activité physique ne sont pas suffisants.
- Risques rares mais sérieux : pancréatite, troubles biliaires.
Ainsi, ces traitements ne corrigent pas le fonctionnement naturel du métabolisme et doivent être accompagnés d’une rééducation alimentaire et d’habitudes de vie adaptées pour garantir une perte de poids durable.
Pourquoi privilégier la stimulation naturelle ?
- Durabilité : le corps apprend à réguler sa satiété et sa combustion sans dépendance médicamenteuse.
- Équilibre global : glycémie, microbiote, sommeil et énergie sont optimisés.
- Sécurité : absence d’effets secondaires majeurs sur le long terme.
En pratique, les agonistes du GLP-1 peuvent compléter la stratégie naturelle dans certains cas, mais ne remplacent jamais une approche globale basée sur l’alimentation, l’activité physique et le mode de vie.
7. Vers une approche durable : réactiver ses hormones naturellement
Le véritable enjeu de la perte de poids n’est pas de “forcer” le corps à maigrir, mais de réapprendre à le laisser réguler son énergie naturellement. Le GLP-1 et le glucagon ne sont pas des interrupteurs que l’on allume avec un médicament: ce sont des messagers métaboliques finement orchestrés qui réagissent à notre hygiène de vie quotidienne.
Rééduquer la satiété
Pour réactiver le GLP-1, il faut restaurer les signaux de satiété que notre mode de vie moderne a perturbés.
Quelques leviers simples mais puissants :
- Manger lentement, en mastiquant bien : cela laisse le temps au GLP-1 d’être libéré dans l’intestin et au cerveau de percevoir la satiété.
- Structurer les repas : trois repas complets par jour limitent les grignotages et favorisent la stabilité hormonale.
Intégrer des aliments riches en protéines et en fibres à chaque repas pour stimuler la libération postprandiale de GLP-1.
En redonnant au corps la possibilité de ressentir la satiété naturelle, on réduit progressivement la dépendance aux signaux externes (régimes, calories, restrictions).
Favoriser la flexibilité métabolique
Le glucagon, quant à lui, agit comme le régulateur énergétique du jeûne. Pour le stimuler, il faut permettre au corps de passer régulièrement en mode “déstockage”.
- Éviter les grignotages constants : chaque ingestion sucrée bloque la libération de glucagon.
- Introduire des périodes de jeûne léger (12 à 14 heures la nuit ou 1 à 2 jours de jeûne intermittent par semaine).
- Bouger à jeun : une marche ou une séance de sport le matin avant le petit-déjeuner stimule le glucagon et la lipolyse.
Ces adaptations simples permettent au métabolisme de redevenir flexible : capable d’utiliser indifféremment le glucose ou les graisses selon les besoins.
Reconnecter le corps et le cerveau
Les hormones digestives n’agissent pas isolément : elles dialoguent en permanence avec le cerveau. Stress, fatigue et émotions influencent directement la sécrétion du GLP-1 et du glucagon.
Ainsi, la régulation du poids est aussi émotionnelle :
- le stress chronique inhibe le GLP-1 et stimule l’appétit,
- la privation de sommeil désynchronise les signaux hormonaux,
- la restriction excessive perturbe la réponse du cerveau à la satiété.
Réapprendre à écouter ses signaux internes – faim, satiété, énergie – est donc une forme de rééducation hormonale à part entière.
Le rôle de l’accompagnement global
Une approche durable nécessite souvent un accompagnement nutritionnel et comportemental. Le professionnel aide à:
- comprendre les besoins individuels,
- ajuster les apports en protéines et en fibres,
- corriger les déséquilibres du microbiote,
- mettre en place des stratégies de gestion du stress et du sommeil.
Ce travail progressif réactive la boucle hormonale naturelle, bien plus efficacement que toute injection ou pilule.
Conclusion : la vraie révolution est hormonale, pas pharmaceutique
La découverte du rôle du GLP-1 et du glucagon marque une avancée majeure : elle prouve que le poids n’est pas qu’une affaire de volonté ou de calories, mais une question d’équilibre hormonal.
Les médicaments agonistes du GLP-1 ont ouvert une voie prometteuse, mais ils ne sont qu’une copie artificielle d’un mécanisme que le corps sait déjà maîtriser. Leur succès repose sur une idée juste — rétablir la satiété et réduire les excès —, mais leur limite est de court-circuiter le système au lieu de le rééduquer.
La véritable solution réside donc dans la stimulation naturelle de ces hormones :
- une alimentation riche en fibres, en protéines et en aliments vivants,
- une activité physique régulière,
- une gestion consciente du stress et du sommeil,
- et le respect des signaux internes du corps.
En agissant sur ces leviers, on ne fait pas qu’activer le GLP-1 et le glucagon : on restaure la symphonie métabolique qui maintient l’équilibre entre satiété, énergie et plaisir de manger.
Autrement dit, la perte de poids durable n’est pas une guerre contre son corps — c’est une reconnexion hormonale par une bonne hygiène de vie.
Références :
- American Psychiatric Association. (2013). Diagnostic and Statistical Manual of Mental Disorders (5th ed.). Arlington, VA: American Psychiatric Publishing.
- Le DSM-5 fournit des définitions détaillées des troubles alimentaires, y compris l’anorexie, la boulimie et l’hyperphagie, ainsi que des informations sur leurs symptômes et critères diagnostiques.
- Fairburn, C. G., & Harrison, P. J. (2003). Eating disorders. The Lancet, 361(9355), 407-416.
- Cet article explore les facteurs de risque des troubles alimentaires et les traitements disponibles. Il examine en particulier les causes psychologiques et biologiques sous-jacentes des troubles alimentaires.
- Lilenfeld, L. R., & Kaye, W. H. (2007). Eating disorders. In M. B. First & J. S. Weissman (Eds.), Clinical Handbook of Psychological Disorders: A Step-by-Step Treatment Manual (4th ed., pp. 419-440). New York: The Guilford Press.
- Un guide approfondi sur les troubles alimentaires, incluant des aspects psychologiques et comportementaux des troubles comme l’anorexie et la boulimie.
- Smink, F. R., van Hoeken, D., & Hoek, H. W. (2012). Epidemiology of eating disorders: Incidence, prevalence and mortality rates. Current Psychiatry Reports, 14(4), 421-427.
- Un article qui examine l’épidémiologie des troubles alimentaires, y compris les prévalences, les facteurs de risque et les comorbidités liées aux TCA.
- Keel, P. K., & Brown, T. A. (2010). Update on the diagnosis and treatment of eating disorders in DSM-5. Journal of Clinical Psychiatry, 71(8), 987-993.
- Cet article discute de l’évolution des critères diagnostiques des troubles alimentaires dans le DSM-5 et des approches thérapeutiques actuelles.
- Muehlenkamp, J. J., & Claes, L. (2014). Non-suicidal self-injury. In B. A. van der Kolk, A. C. McFarlane, & L. Weisaeth (Eds.), Trauma and Recovery (pp. 377-391). New York: Guilford Press.
- Bien que cet article soit centré sur l’automutilation, il fournit des informations pertinentes sur la manière dont les personnes vivant avec des traumatismes peuvent utiliser des comportements alimentaires pour gérer la douleur émotionnelle.
- Polivy, J., & Herman, C. P. (2002). Causes of eating disorders. Annual Review of Psychology, 53, 187-213.
- Une revue complète des causes des troubles alimentaires, incluant des discussions sur les facteurs psychologiques, biologiques et socioculturels.
- Trace, S. E., & Bulik, C. M. (2015). Genetics of eating disorders. Current Diabetes Reports, 15(1), 3.
- Un article approfondissant les facteurs génétiques des troubles alimentaires, en particulier la prédisposition familiale et les recherches sur les mutations génétiques liées à ces troubles.