Hyperperméabilité intestinale : un déclencheur des intolérances alimentaires et des maladies auto-immunes
Rédaction : Anne-Christine DUSS, Nutritionniste – Genève
L’hyperperméabilité intestinale : qu’est-ce que c’est?
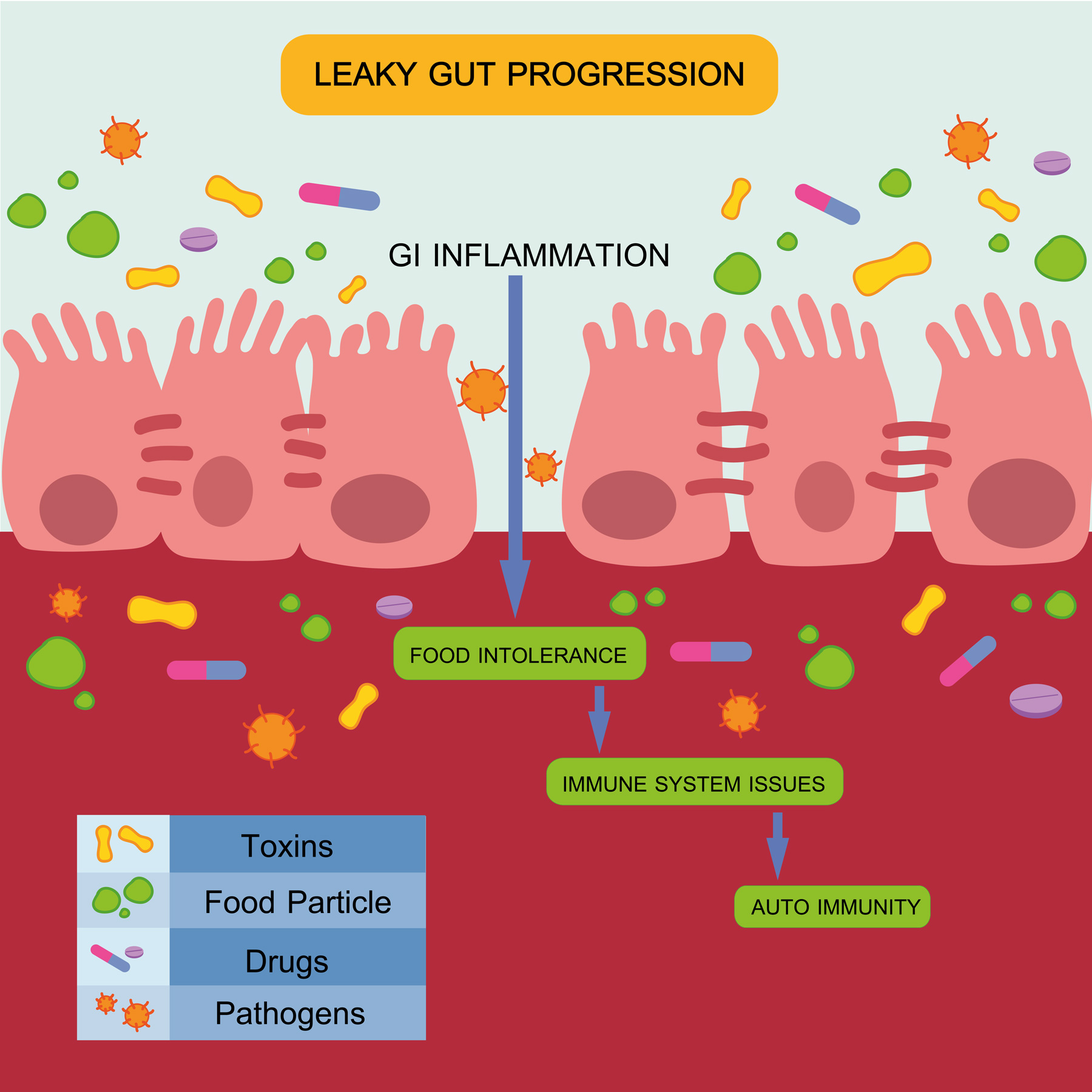
L’hyperperméabilité intestinale, appelée « leaky gut Syndrome » en anglais, désigne une condition dans laquelle la paroi intestinale devient plus perméable que la normale, permettant à des substances qui de devrait pas passer la barrière intestinale de pénétrer dans la circulation sanguine. Cela perturbe l’équilibre du système digestif et peut entraîner une série de réactions inflammatoires et immunitaires. Voici un aperçu des mécanismes biologiques et physiologiques impliqués :
1. Les jonctions serrées et leur rôle dans l’intestin
Les jonctions serrées (ou tight junctions) sont des structures protéiques situées entre les cellules épithéliales de la paroi intestinale. Ces jonctions ont pour fonction de maintenir une barrière étanche et de réguler le passage des substances à travers l’intestin. Elles jouent un rôle crucial dans l’intégrité de la muqueuse intestinale, empêchant les microbes, les toxines et les antigènes alimentaires de pénétrer dans la circulation sanguine.
- Fonction normale : Les jonctions serrées permettent un passage sélectif, autorisant les nutriments et l’eau à traverser l’intestin tout en bloquant les particules plus grandes, telles que les bactéries et les toxines.
2. Dysfonction des jonctions serrées : L’hyperperméabilité
L’hyperperméabilité intestinale survient lorsque ces jonctions serrées deviennent dysfonctionnelles. Cela peut être causé par des facteurs internes ou externes, tels que des infections, une alimentation inflammatoire, le stress, des déséquilibres microbiens ou des toxines.
- Impact : Lorsque les jonctions serrées se relâchent ou s’affaiblissent, elles permettent à des substances non souhaitées, comme des bactéries, des toxines ou des antigènes alimentaires, de traverser la paroi intestinale et d’entrer dans le sang. Ce phénomène est appelé translocation ou « fuite » de l’intestin.
3. Les antigènes alimentaires, bactéries et toxines dans la circulation systémique
Une fois que des substances non filtrées pénètrent dans la circulation, elles peuvent provoquer une réaction du système immunitaire. Les antigènes alimentaires (comme les protéines non digérées), les toxines produites par des bactéries pathogènes et même des fragments de bactéries peuvent être perçus comme des agents étrangers par l’organisme.
- Réponse immunitaire : Le système immunitaire reconnaît ces substances comme des « intrus » et active une réponse inflammatoire pour les éliminer. Cependant, cette activation constante du système immunitaire peut entraîner une inflammation systémique, même à faible niveau, contribuant à des maladies chroniques.
4. Inflammation chronique et conséquences
Lorsque l’inflammation déclenchée par le système immunitaire devient chronique, elle peut affecter plusieurs systèmes du corps, notamment :
- Système digestif : L’inflammation peut perturber encore plus la fonction intestinale, exacerbant les symptômes tels que la douleur abdominale, les ballonnements, la diarrhée ou la constipation.
- Système immunitaire : Une inflammation persistante peut affaiblir le système immunitaire, le rendant moins efficace pour combattre d’autres infections ou maladies.
- Système nerveux : L’inflammation intestinale peut affecter l’axe intestin-cerveau, ce qui a des répercussions sur la santé mentale, notamment en contribuant à des troubles comme l’anxiété, la dépression ou même des troubles de l’humeur.
5. Facteurs contributifs à l’hyperperméabilité intestinale
L’hyperperméabilité intestinale peut être exacerbée par plusieurs facteurs :
- Alimentation déséquilibrée : Une consommation excessive de sucres raffinés, de graisses saturées, d’alcool, ou encore d’additifs alimentaires peut altérer les jonctions serrées. De plus, certains aliments comme le gluten ou les produits laitiers peuvent jouer un rôle dans l’irritation de la paroi intestinale chez certaines personnes.
- Stress chronique : Le stress prolongé peut altérer la fonction du système immunitaire et perturber l’intégrité de la barrière intestinale.
- Infections et dysbiose : Des déséquilibres dans la flore intestinale (dysbiose), causés par des infections bactériennes ou une mauvaise gestion des probiotiques, peuvent jouer un rôle central dans la perturbation de la fonction des jonctions serrées.
6. Impact sur la santé globale
L’hyperperméabilité intestinale est de plus en plus associée à des conditions de santé variées, telles que :
- Troubles inflammatoires : Comme les maladies auto-immunes, les maladies inflammatoires chroniques de l’intestin (MICI), telles que la maladie de Crohn et la colite ulcéreuse.
- Maladies métaboliques : L’inflammation systémique peut contribuer à l’obésité, au diabète de type 2 et aux maladies cardiovasculaires.
- Troubles neurologiques : En raison de l’axe intestin-cerveau, l’inflammation intestinale peut affecter le fonctionnement du cerveau, contribuant à des troubles comme la dépression, l’anxiété ou des troubles cognitifs.
7. Approches thérapeutiques
Pour corriger l’hyperperméabilité intestinale, plusieurs approches sont recommandées :
- Alimentation anti-inflammatoire : Favoriser des aliments riches en fibres, en antioxydants et en acides gras oméga-3, tout en réduisant les aliments inflammatoires.
- Probiotiques et prébiotiques : Améliorer l’équilibre du microbiote intestinal pour soutenir la régénération de la muqueuse intestinale.
- Gestion du stress : Pratiquer des techniques de relaxation comme la méditation, la respiration profonde et le yoga pour réduire le stress.
- Suppression des déclencheurs : Identifier et éviter les aliments ou substances qui provoquent une réaction inflammatoire (par exemple, le gluten, le lait ou certains additifs alimentaires).
L’hyperperméabilité intestinale est un processus complexe, mais en comprenant ses mécanismes biologiques et physiologiques, il est possible de prendre des mesures pour restaurer la santé intestinale et réduire les effets de l’inflammation chronique sur le corps.
Intolérances alimentaires secondaires : Lien avec l’hyperperméabilité intestinale
Les intolérances alimentaires secondaires sont un phénomène souvent observé chez les personnes souffrant d’hyperperméabilité intestinale. En raison de la perturbation de la barrière intestinale, le système immunitaire réagit de manière excessive à des aliments qui étaient auparavant bien tolérés, ce qui peut entraîner des symptômes variés de malaises digestifs, de fatigue, de douleurs chroniques, ou de troubles cutanés. L’hyperperméabilité intestinale crée un terrain propice à l’apparition ou à l’aggravation de ces intolérances. Voici comment ce processus se déroule.
1. Protéines alimentaires mal digérées et passage à travers la barrière intestinale
Dans un intestin sain, la digestion des protéines se fait de manière optimale. Les enzymes digestives décomposent les protéines alimentaires en acides aminés, les composants de base qui peuvent être absorbés facilement par l’intestin grêle. Cependant, lorsque l’intégrité de la barrière intestinale est compromise, des fragments de protéines mal digérées, comme le gluten (blé) ou la caséine (lait), peuvent traverser les jonctions serrées et pénétrer dans la circulation sanguine.
- Exemple avec le gluten et la caséine :
- Le gluten est une protéine présente dans le blé et d’autres céréales. Lorsque l’intestin est perméable, des fragments de gluten non digérés peuvent pénétrer dans la circulation, déclenchant une réaction immunitaire dans l’organisme.
- La caséine, protéine présente dans le lait et ses dérivés, fonctionne de manière similaire. Si elle ne se dégrade pas correctement, des peptides (petites protéines) de caséine peuvent traverser la barrière intestinale et devenir des antigènes, activant ainsi une réponse immunitaire.
2. Réponse immunitaire excessive : Sensibilisation croisée
Une fois que des fragments de protéines alimentaires non digérées (comme le gluten ou la caséine) pénètrent dans la circulation sanguine, le système immunitaire les reconnaît comme des substances étrangères. Cela déclenche une réponse immunitaire qui peut être amplifiée si l’organisme est déjà sensibilisé à ces protéines. Cette sensibilisation conduit à une réaction excessive à des aliments qui étaient autrefois tolérés sans problème.
La sensibilisation croisée est un phénomène où le système immunitaire réagit à un aliment en particulier, mais cette réaction s’étend à d’autres aliments ayant des structures similaires. Cela peut aggraver les symptômes d’intolérances alimentaires et rendre la gestion des réactions immunitaires plus complexe.
- Exemple de sensibilisation croisée :
- Une personne ayant une réaction immunitaire au gluten peut également développer une réaction similaire à d’autres céréales contenant des protéines similaires, comme le seigle ou l’orge.
- De même, une intolérance à la caséine peut également inclure des réactions à d’autres protéines animales (comme celles présentes dans les œufs ou la viande), exacerbant ainsi les symptômes.
Cette réponse immunitaire peut entraîner une inflammation systémique, agissant non seulement sur l’intestin, mais aussi sur d’autres organes, contribuant à des symptômes extragastro-intestinaux tels que des douleurs articulaires, des migraines, ou des problèmes cutanés comme l’eczéma.
3. Inflammation chronique et cercle vicieux
L’inflammation causée par l’hyperperméabilité intestinale joue un rôle central dans l’aggravation des intolérances alimentaires. Une fois que des fragments de protéines ou des toxines pénètrent dans la circulation sanguine, le système immunitaire réagit de manière exacerbée, produisant des cytokines pro-inflammatoires. Les cytokines pro-inflammatoires sont des protéines produites par le système immunitaire qui favorisent l’inflammation. Elles jouent un rôle clé dans la réponse de l’organisme aux infections, aux blessures ou aux maladies, en activant les cellules immunitaires et en stimulant la production d’autres médiateurs inflammatoires. Cependant, une production excessive de cytokines pro-inflammatoires peut être impliquée dans des pathologies chroniques (maladies auto-immunes et troubles métaboliques).
Cette inflammation locale au niveau de l’intestin, peut se propager à l’ensemble du corps, affectant plusieurs systèmes physiologiques.
- Aggravation de la digestion : L’inflammation chronique altère encore davantage la fonction digestive, rendant l’absorption des nutriments plus difficile et exacerbant les symptômes d’intolérances alimentaires. Par exemple, les personnes souffrant d’inflammation intestinale peuvent avoir des difficultés à digérer certains aliments, entraînant des ballonnements, des douleurs abdominales, des nausées, ou des diarrhées.
- Cercle vicieux : L’inflammation peut altérer les jonctions serrées de l’intestin, créant davantage de fuites, ce qui permet à encore plus de fragments alimentaires et de toxines de pénétrer dans la circulation. Cela intensifie la réponse immunitaire, entraînant davantage d’inflammation. Ce processus peut devenir un cercle vicieux où l’hyperperméabilité intestinale et les intolérances alimentaires se nourrissent mutuellement.
4. Symptômes et conséquences des intolérances alimentaires secondaires
Les intolérances alimentaires secondaires sont souvent associées à des symptômes variés, dont :
- Symptômes digestifs : Ballonnements, douleurs abdominales, crampes, diarrhée ou constipation.
- Symptômes cutanés : Éruptions cutanées, eczéma, démangeaisons.
- Symptômes neurologiques : Fatigue, migraines, brouillard mental, anxiété, dépression.
- Symptômes immunitaires : Infections fréquentes, réactions allergiques, douleurs articulaires.
Ces symptômes peuvent s’aggraver avec l’exposition répétée à des aliments spécifiques, même ceux qui étaient tolérés auparavant.
5. Prise en charge et traitement des intolérances alimentaires secondaires
La gestion des intolérances alimentaires secondaires nécessite une approche multidimensionnelle pour traiter à la fois l’hyperperméabilité intestinale et les réponses immunitaires exagérées.
- Réparation de la barrière intestinale : Les traitements visant à restaurer l’intégrité de la paroi intestinale peuvent inclure des régimes alimentaires anti-inflammatoires, la prise de probiotiques et de prébiotiques, ainsi que des suppléments comme le L-glutamine ou la N-acétylcystéine, qui soutiennent la régénération des cellules intestinales.
- Élimination provisoire ou définitive des déclencheurs alimentaires : Identifier et éviter les aliments qui exacerbent l’inflammation et qui traversent facilement la barrière intestinale (par exemple, gluten, produits laitiers, aliments riches en sucres ou en graisses saturées) peut être crucial pour réduire les symptômes.
- Régulation du système immunitaire : Des approches comme l’optimisation du microbiote intestinal, la gestion du stress, et l’utilisation d’anti-inflammatoires naturels (par exemple, curcuma, oméga-3) peuvent contribuer à moduler la réponse immunitaire et réduire l’inflammation chronique.
En traitant à la fois l’hyperperméabilité intestinale et les intolérances alimentaires secondaires, il est possible de restaurer un équilibre fonctionnel dans le système digestif et d’améliorer la santé globale de la personne.
Maladies auto-immunes et intestin perméable : Le rôle clé de l’hyperperméabilité intestinale
L’hyperperméabilité intestinale, souvent appelée « intestin perméable », joue un rôle essentiel dans l’émergence et l’aggravation des maladies auto-immunes. Ces maladies se caractérisent par une réponse immunitaire anormale où le système immunitaire attaque par erreur les tissus sains de l’organisme. L’intestin perméable crée un environnement propice à cette dysfonction en permettant à des antigènes et des toxines de pénétrer dans la circulation sanguine, où ils peuvent interagir avec le système immunitaire de manière délétère.
1. Mimétisme moléculaire et déclenchement des réponses auto-immunes
Le mimétisme moléculaire est un phénomène clé dans le lien entre l’hyperperméabilité intestinale et les maladies auto-immunes. Les antigènes étrangers, comme des fragments de protéines alimentaires (gluten, caséine), des toxines ou des bactéries, qui traversent une paroi intestinale altérée, peuvent posséder des structures chimiques similaires à celles des cellules humaines. Lorsqu’ils entrent en contact avec le système immunitaire, ce dernier peut les identifier à tort comme des menaces.
Le système immunitaire, en réagissant contre ces antigènes étrangers, peut également attaquer par erreur des structures similaires présentes dans l’organisme, ce qui déclenche une réponse auto-immune. Voici deux exemples courants où ce processus est observé :
- Maladie cœliaque : Dans la maladie cœliaque, le gluten (une protéine présente dans le blé) est mal digéré et traverse la paroi intestinale. Le système immunitaire réagit contre le gluten, mais cette réaction entraîne aussi des attaques contre la paroi intestinale elle-même, provoquant une inflammation et une altération des villosités intestinales.
- Thyroïdite de Hashimoto : Dans cette maladie auto-immune, le mimétisme moléculaire entre certaines protéines bactériennes et les cellules de la glande thyroïde peut conduire à une attaque des cellules thyroïdiennes, provoquant une hypothyroïdie.
2. Activation chronique du système immunitaire et pathologies auto-immunes
Lorsqu’il y a une hyperperméabilité intestinale, l’exposition continue à des antigènes étrangers comme des fragments de protéines alimentaires, des toxines, ou des bactéries, entraîne une activation chronique du système immunitaire. Cela pousse le système immunitaire à réagir de manière excessive, en déclenchant une inflammation persistante dans l’ensemble de l’organisme. Une réponse immune continue peut engendrer plusieurs pathologies auto-immunes, comme :
- Lupus érythémateux systémique (LES) : Une maladie auto-immune complexe où le système immunitaire attaque plusieurs tissus, y compris la peau, les articulations, et les reins.
- Polyarthrite rhumatoïde : Dans cette maladie, le système immunitaire attaque les articulations, entraînant des douleurs, des gonflements et des déformations.
- Sclérose en plaques : Une maladie où le système immunitaire détruit la myéline, la substance qui entoure et protège les nerfs du cerveau et de la moelle épinière, ce qui entraîne des symptômes neurologiques.
3. Le microbiote intestinal et son influence sur l’hyperperméabilité
Le microbiote intestinal joue un rôle crucial dans le maintien de l’intégrité de la barrière intestinale. Un déséquilibre du microbiote, connu sous le nom de dysbiose, peut accentuer l’hyperperméabilité intestinale en plusieurs façons :
- Production d’endotoxines : Les bactéries pathogènes et les bactéries en excès dans un microbiote déséquilibré peuvent produire des endotoxines (notamment des lipopolysaccharides, LPS), qui perturbent encore la fonction de la paroi intestinale. Ces endotoxines peuvent traverser la barrière intestinale fragilisée et entrer dans la circulation, exacerbant l’inflammation et la perméabilité.
- Altération des mécanismes de défense de l’intestin : Une dysbiose intestinale modifie les mécanismes de défense naturels de l’intestin, comme la production de mucus et l’activité des jonctions serrées, augmentant ainsi la perméabilité intestinale.
En d’autres termes, un microbiote déséquilibré peut être à la fois une cause et une conséquence de l’hyperperméabilité intestinale, amplifiant la vulnérabilité du corps à des maladies auto-immunes.
4. Causes principales de l’hyperperméabilité intestinale
L’hyperperméabilité intestinale peut être causée par plusieurs facteurs environnementaux, alimentaires et physiopathologiques qui affectent la fonction intestinale. Les causes principales incluent :
- Alimentation déséquilibrée : Une alimentation riche en aliments ultra-transformés, en sucres raffinés, en gluten, en produits laitiers et en alcool fragilise la barrière intestinale. Ces substances favorisent une inflammation chronique et peuvent également nourrir des bactéries pathogènes dans le microbiote, aggravant la dysbiose.
- Stress chronique : Le stress chronique augmente la production de cortisol, une hormone du stress qui peut avoir un effet direct sur les jonctions serrées des cellules intestinales, augmentant leur perméabilité. Le stress peut également déséquilibrer le microbiote, exacerbant ainsi l’hyperperméabilité.
- Dysbiose intestinale : Le déséquilibre des bactéries intestinales favorise la croissance de bactéries pathogènes et la production d’endotoxines. Cela fragilise la barrière intestinale et augmente l’inflammation systémique.
- Infections intestinales : Les infections bactériennes, virales ou parasitaires peuvent endommager la paroi intestinale, perturbant les jonctions serrées et augmentant la perméabilité. Cela peut également déclencher une réponse immunitaire exacerbée.
- Toxines environnementales : Les pesticides, métaux lourds, et additifs alimentaires peuvent aggraver les dommages à la paroi intestinale et augmenter l’inflammation. Ces toxines peuvent non seulement affecter l’intestin, mais aussi interférer avec le système immunitaire, favorisant des réponses auto-immunes.
5. Prise en charge et prévention
La gestion de l’hyperperméabilité intestinale passe par une approche holistique qui inclut des modifications alimentaires et du mode de vie, ainsi que des traitements ciblés :
- Régime anti-inflammatoire : Un régime riche en fruits, légumes, fibres, acides gras oméga-3 et probiotiques peut soutenir la réparation de la paroi intestinale et aider à rééquilibrer le microbiote.
- Réduction du stress : La gestion du stress à travers des techniques de relaxation, de méditation ou de yoga peut avoir un impact direct sur la santé intestinale.
- Éviter les toxines : Minimiser l’exposition aux toxines environnementales (pesticides, métaux lourds) et aux aliments transformés est essentiel pour protéger la fonction intestinale.
- Traitements médicaux : Dans certains cas, des traitements comme les probiotiques, la L-glutamine, ou d’autres suppléments visant à renforcer les jonctions serrées ou réduire l’inflammation peuvent être recommandés.
En résumé, l’hyperperméabilité intestinale joue un rôle clé dans le développement et l’aggravation des maladies auto-immunes en facilitant l’entrée de substances étrangères dans la circulation sanguine et en activant une réponse immunitaire anormale. Une gestion proactive de l’hyperperméabilité intestinale, combinée à un mode de vie sain et une attention particulière au microbiote intestinal, peut aider à prévenir ou à modérer l’apparition de ces pathologies.
Tests de laboratoire pour le diagnostic de l’intestin perméable
-
Test de la lactulose/mannitol
- But : Ce test mesure la perméabilité intestinale en utilisant deux sucres, la lactulose et le mannitol. Le mannitol est facilement absorbé par un intestin sain, tandis que la lactulose, étant plus grande, devrait être moins absorbée. Si la lactulose traverse facilement la barrière intestinale, cela indique une perméabilité accrue.
- Procédure : Le patient boit une solution contenant les deux sucres. La quantité de chaque sucre qui apparaît dans l’urine est mesurée pendant les 6 à 8 heures suivant l’ingestion. Un rapport élevé de lactulose par rapport au mannitol suggère une hyperperméabilité intestinale.
-
Test des anticorps contre les protéines alimentaires (IgG, IgA, IgM)
- But : Ce test mesure les niveaux d’anticorps contre des protéines alimentaires spécifiques (par exemple, le gluten, la caséine, les œufs, le soja) dans le sang. Une production accrue d’anticorps peut suggérer que des protéines non digérées traversent la paroi intestinale, ce qui pourrait être un signe de perméabilité accrue.
- Procédure : Un échantillon de sang est prélevé pour analyser la présence d’anticorps. Des niveaux élevés d’IgG ou d’IgA spécifiques aux aliments peuvent indiquer une intolérance alimentaire ou une réponse immunitaire exacerbée en raison de l’hyperperméabilité intestinale.
-
Mesure des endotoxines ou lipopolysaccharides (LPS) dans le sang
- But : Les endotoxines, comme les lipopolysaccharides (LPS), sont des composants de la paroi cellulaire de certaines bactéries intestinales. Lorsque la barrière intestinale est altérée, les LPS peuvent pénétrer dans la circulation sanguine, ce qui entraîne une inflammation systémique.
- Procédure : Un prélèvement sanguin est effectué pour mesurer la concentration de LPS dans le sang. Un taux élevé de LPS peut être un indicateur d’hyperperméabilité intestinale.
-
Test de zonuline
- But : La zonuline est une protéine qui régule les jonctions serrées entre les cellules intestinales. Une augmentation des niveaux de zonuline dans le sang ou dans les selles est souvent associée à une hyperperméabilité intestinale.
- Procédure : Un échantillon de sang ou de selles est prélevé pour mesurer les niveaux de zonuline. Des niveaux élevés de zonuline peuvent indiquer une dysfonction de la barrière intestinale.
-
Analyse du microbiote intestinal (profil microbien)
- But : Un microbiote intestinal déséquilibré (dysbiose) est souvent impliqué dans l’hyperperméabilité intestinale. Un profil microbien détaillé peut identifier les bactéries pathogènes et bénéfiques présentes dans l’intestin, permettant d’évaluer leur impact sur la perméabilité intestinale.
- Procédure : Un échantillon de selles est prélevé pour une analyse de la diversité et de la composition du microbiote intestinal. Cela peut révéler des déséquilibres, comme une prolifération de bactéries pathogènes, qui pourraient contribuer à l’hyperperméabilité.
-
Test des acides organiques urinaires
- But : Ce test mesure les niveaux d’acides organiques dans les urines, qui peuvent indiquer un métabolisme anormal des toxines et une fonction intestinale altérée. Des niveaux anormaux d’acides comme les acides gras à chaîne courte (produits par les bactéries intestinales) ou d’autres métabolites peuvent être des signes de dysbiose ou d’inflammation intestinale.
- Procédure : Un échantillon d’urine est prélevé sur 24 heures pour mesurer les acides organiques. Des profils anormaux peuvent suggérer des problèmes d’hyperperméabilité intestinale ou d’autres dysfonctionnements métaboliques liés à l’intestin.
Tests complémentaires pour évaluer les conséquences de l’intestin perméable
- Profil inflammatoire (CRP, cytokines) : Une inflammation systémique est souvent observée en cas d’intestin perméable. Les tests de la protéine C-réactive (CRP) et des cytokines inflammatoires (comme l’IL-6 ou le TNF-alpha) peuvent aider à évaluer le niveau d’inflammation dans le corps, ce qui est fréquent dans les conditions liées à l’hyperperméabilité intestinale.
- Bilan hormonal : L’hyperperméabilité intestinale peut également affecter la gestion des hormones, notamment les hormones thyroïdiennes ou les hormones du stress comme le cortisol. Des analyses sanguines peuvent être utiles pour évaluer ces paramètres.
Les tests de laboratoire pour évaluer l’hyperperméabilité intestinale peuvent fournir des informations cruciales pour comprendre la santé intestinale et ses impacts sur le système immunitaire. Une combinaison de tests, incluant la lactulose/mannitol, la mesure de la zonuline, et l’analyse des anticorps alimentaires ou du microbiote, permet une évaluation approfondie du syndrome de l’intestin perméable et de ses conséquences sur la santé générale.
Quelques pistes pour restaurer l’intégrité de la barrière intestinale
- Adopter une alimentation équilibrée
- Inclure des aliments variés et naturels pour soutenir la santé de la muqueuse intestinale.
- Réduire les aliments transformés et ceux susceptibles d’irriter l’intestin.
- Soutien nutritionnel ciblé
- Consommer des nutriments qui favorisent la réparation de la barrière intestinale.
- Envisager l’utilisation de compléments pour aider à rétablir l’équilibre si nécessaire.
- Gestion du stress
- Intégrer des pratiques de relaxation dans son quotidien, comme des exercices de respiration ou des activités apaisantes.
- Favoriser un mode de vie sain
- Veiller à une hydratation adéquate et à un sommeil de qualité, essentiels pour la régénération de l’organisme.
- Réduire l’exposition aux toxines
- Privilégier des choix plus naturels, autant dans l’alimentation que dans l’environnement, pour limiter les substances nocives.
Vers une approche intégrée
L’hyperperméabilité intestinale n’est pas une fatalité. En adoptant une approche globale combinant alimentation, gestion du stress, et soutien micronutritionnel, il est possible de restaurer l’intégrité de la barrière intestinale. Cette démarche peut prévenir l’apparition de pathologies auto-immunes et limiter les intolérances secondaires, offrant ainsi une meilleure qualité de vie.
Références
- Fasano, A. (2001). « Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. » Physiological Reviews, 81(1), 1-20.
- Cet article fondamental d’Antonio Fasano, l’un des principaux chercheurs sur la zonuline, décrit le rôle de cette protéine dans la régulation de la perméabilité intestinale et ses implications dans diverses pathologies, y compris les maladies auto-immunes.
- Miele, E., et al. (2009). « Increased intestinal permeability in patients with Crohn’s disease and their unaffected relatives. » Gut, 58(1), 31-37.
- Cette étude examine le lien entre la perméabilité intestinale et la maladie de Crohn, en mettant en évidence comment la perméabilité accrue peut être une caractéristique partagée par les patients et leurs proches.
- Vanheel, H., et al. (2011). « The role of the intestinal barrier in the pathogenesis of irritable bowel syndrome and inflammatory bowel diseases. » Alimentary Pharmacology & Therapeutics, 34(2), 208-214.
- Cet article explore le rôle de la barrière intestinale dans le développement de troubles digestifs tels que le syndrome de l’intestin irritable et les maladies inflammatoires chroniques de l’intestin (MICI).
- Vazquez-Castellanos, J. F., et al. (2015). « The intestinal microbiota of patients with irritable bowel syndrome is dysbiotic and modulated by the use of probiotics. » Gastroenterology, 149(2), 397-406.
- Cette étude examine le microbiote intestinal des patients atteints de syndrome de l’intestin irritable (SII) et l’impact de l’utilisation de probiotiques, ce qui peut offrir des pistes pour traiter la dysbiose et l’hyperperméabilité.
- Brestoff, J. R., et al. (2015). « The microbiome and host immune system: a love-hate relationship. » Nature Reviews Immunology, 15(3), 174-186.
- Cet article aborde la relation complexe entre le microbiote intestinal et le système immunitaire, en discutant de la manière dont l’hyperperméabilité intestinale peut perturber cette relation et contribuer à l’inflammation et aux maladies auto-immunes.
- Parks, R. A., et al. (2018). « Intestinal permeability in systemic disease. » Gastroenterology Clinics of North America, 47(4), 549-565.
- Cette revue fournit un aperçu approfondi du rôle de l’hyperperméabilité intestinale dans diverses maladies systémiques, y compris les maladies auto-immunes, les troubles digestifs et les pathologies métaboliques.
- Németh, M., et al. (2016). « The role of intestinal permeability in autoimmune diseases. » Current Diabetes Reviews, 12(3), 205-212.
- L’article examine comment l’altération de la perméabilité intestinale peut jouer un rôle clé dans le développement des maladies auto-immunes, avec un focus particulier sur la relation entre l’intestin perméable et les troubles endocriniens comme la thyroïdite de Hashimoto.
- Bourdet-Sicard, R., et al. (2003). « Effects of diet and probiotics on the intestinal microbiota, gut permeability, and health. » Current Opinion in Clinical Nutrition & Metabolic Care, 6(5), 551-556.
- Cet article explore l’impact de l’alimentation, des régimes spéciaux et des probiotiques sur la perméabilité intestinale et la santé globale, en soulignant l’importance de maintenir une barrière intestinale intacte.
- Camilleri, M. (2019). « Leaky gut: mechanisms, measurement and clinical implications. » European Journal of Clinical Investigation, 49(8), e13146.
- Une revue récente sur le syndrome de l’intestin perméable, qui traite des mécanismes biologiques sous-jacents, des méthodes de mesure de la perméabilité intestinale et des implications cliniques pour les troubles digestifs et les maladies systémiques.
- Hughes, P. A., et al. (2014). « Increased intestinal permeability in patients with irritable bowel syndrome. » Gut, 63(3), 475-481.
- Cette étude montre que l’hyperperméabilité intestinale est un phénomène courant chez les patients atteints du syndrome de l’intestin irritable (SII), soulignant les liens entre cette condition et la dysfonction de la barrière intestinale.
Sources supplémentaires :
- Books :
- Fasano, A., et al. (2012). Celiac Disease: A Hidden Epidemic. Wiley-Blackwell.
- Mayer, E. A. (2011). The Mind-Gut Connection. HarperCollins.